иҝ‘жңҹ����пјҢдәҝдёҮе…Ҳз”ҹMRзҗҶеӯҰйҷўиө„ж–ҷз”ҹзү©еӯҰй’»з ”жүҖдёҺдёҠжө·дәӨйҖҡеӨ§еӯҰеҗҲдҪңеӣўйҳҹеңЁгҖҠе…Ҳиҝӣиө„ж–ҷгҖӢпјҲAdvanced MaterialsпјүйўҒеҸ‘дәҶйўҳдёәDNA-programmed stem cell niches via orthogonal extracellular vesicle-cell communicationsзҡ„й’»з ”и®әж–Ү�����гҖӮиҜҘи®әж–ҮеҸ‘еұ•дәҶдёҖз§ҚDNAзј–з Ғзҡ„дәәдёәвҖңй…ҚдҪ“-еҸ—дҪ“вҖқзі»з»ҹз”ЁдәҺеҸҜзј–зЁӢи°ғжҺ§з»ҶиғһиЎЁеӣҠжіЎдёҺз»Ҷиғһй—ҙзҡ„жӯЈдәӨйҖҡи®Ҝ����пјҢ并жһ„е»әдәҶеҹәдәҺиҜҘзі»з»ҹзҡ„е№Із»Ҷиғһеҫ®зҺҜеўғ����пјҢеҚівҖңе№Із»ҶиғһйҫӣвҖқ����пјҢеҸҜж”ҜжҢҒзҒөй•ҝзұ»еҠЁзү©йӣҢжҖ§з”ҹж®–е№Із»ҶиғһдҪ“иЎЁиҮӘжҲ‘жӣҙж–°дёҺе№ІжҖ§з»ҙжҢҒ����пјҢдёәе№Із»Ҷиғһе·ҘзЁӢеҢ–еҲ©з”ЁжҸҗдҫӣдәҶж–°е·Ҙе…·�����гҖӮдәҝдёҮе…Ҳз”ҹMRзҗҶеӯҰйҷўиө„ж–ҷз”ҹзү©еӯҰй’»з ”жүҖжқҺжұҹй’»з ”е‘ҳдёҺдёҠжө·дәӨйҖҡеӨ§еӯҰBio-Xй’»з ”йҷўеҗҙйҷ…ж•ҷжҺҲдёәи®әж–Үе…ұеҗҢйҖҡи®ҜдҪңиҖ…�����гҖӮ
2009е№ҙ����пјҢеҗҙйҷ…ж•ҷжҺҲеӣўйҳҹеҲқж¬ЎеңЁжҲҗе№ҙе“әд№іеҠЁзү©еҚөе·ўеҶ…еҸ‘зҺ°дәҶйӣҢжҖ§з”ҹж®–е№Із»Ҷиғһ����пјҢиҝҷдёҖеҸ‘жӯӨеҲ»з”ҹж®–з”ҹзү©еӯҰдёҺеҶҚз”ҹеҢ»еӯҰзӯүйўҶеҹҹжңүжІүиҰҒзҡ„科еӯҰж„ҸжҖқдёҺе®Ҫжіӣзҡ„еҲ©з”ЁиҝңжҷҜ�����гҖӮ然иҖҢиҮід»Ҡ����пјҢйӣҢжҖ§з”ҹж®–е№Із»Ҷиғһзҡ„дҪ“иЎЁе·ҘзЁӢеҢ–йҖ е°ұдёҺеҲ·ж–°дҫқ然еӯҳеңЁиҜёеӨҡжҢ‘жҲҳ�����гҖӮиҝҷйҮҚиҰҒжҳҜз”ұдәҺе№Із»ҶиғһдёҺз»ҶиғһиЎЁзҺҜеўғд№Ӣй—ҙзҡ„дҝЎжҒҜдёҺзү©иҙЁдә’жҚўеҜ№з»Ҷиғһе‘Ҫиҝҗи°ғжҺ§иҮіе…іжІүиҰҒеҸҲжһҒдёәеӨҚжқӮ����пјҢжҲ‘们иҝҳдёҚи¶ій’ҲеҜ№иҝҷдёҖиҝҮзЁӢзҡ„зІҫзЎ®и°ғжҺ§дјҺдҝ©�����гҖӮз»ҶиғһиЎЁеӣҠжіЎдҪңдёәз»ҶиғһжҺ’жі„зҡ„дёҖзұ»еӨ©з„¶зәізұіеӣҠжіЎ����пјҢиғҪеӨҹжү“еҢ…дј йҖ’еӨҡз§Қз”ҹзү©жҙ»жҖ§зү©иҙЁ����пјҢеҰӮиӣӢзҷҪиҙЁгҖҒи„ӮиҙЁгҖҒж ёй…ёзӯү�����гҖӮиҝҷжҳҜз”ҹзү©иҝӣеҢ–дёҠе®Ҳж—§зҡ„дёҖз§Қз»ҶиғһеҸҠзү©з§Қй—ҙйҖҡи®ҜжңәйҖ �����гҖӮжІүзј–зЁӢз»ҶиғһиЎЁеӣҠжіЎдёҺз»Ҷиғһзҡ„зӣёдә’дҪңз”ЁеҸҜд»ҘдёәдҪ“иЎЁз»Ҷиғһе·ҘзЁӢе’Ңз»Ҷиғһеӣһи·Ҝжһ„е»әжҸҗдҫӣж–°зҡ„е·Ҙе…·�����гҖӮ
иҝ‘е№ҙжқҘ����пјҢDNAзәізұіжҠҖжңҜзҡ„еҸ‘еұ•дёәй’»з ”иҖ…们жҸҗдҫӣдәҶдёҖз§ҚеҹәдәҺзўұеҹәдә’иЎҘй…ҚеҜ№еҮҶеҲҷзҡ„ж–№ејҸжқҘзј–зЁӢи°ғжҺ§еҲҶжӯ§зҡ„еӨ©з„¶/дәәдёәиө„ж–ҷд№Ӣй—ҙзҡ„зӣёдә’дҪңз”Ё����пјҢиғҪеӨҹе®һзҺ°д»Һзәізұійў—зІ’еҲ°жҙ»з»Ҷиғһзӯүеҗ„зұ»иө„ж–ҷзҡ„зІҫзЎ®з»„иЈ…дёҺз©әй—ҙжҺ’еёғ�����гҖӮеңЁжӯӨеёғжҷҜдёӢ����пјҢй’»з ”еӣўйҳҹи®ҫжғіпјҡеҸҜеҗҰеҲ©з”ЁDNAз»“жһ„зј–зЁӢи°ғжҺ§з»ҶиғһиЎЁеӣҠжіЎдёҺз»Ҷиғһй—ҙзҡ„йҖҡи®Ҝ����пјҢз”ЁдәҺжһ„е»әе®ҡйҖ еҢ–зҡ„е№Із»Ҷиғһеҫ®зҺҜеўғ�����пјҹ
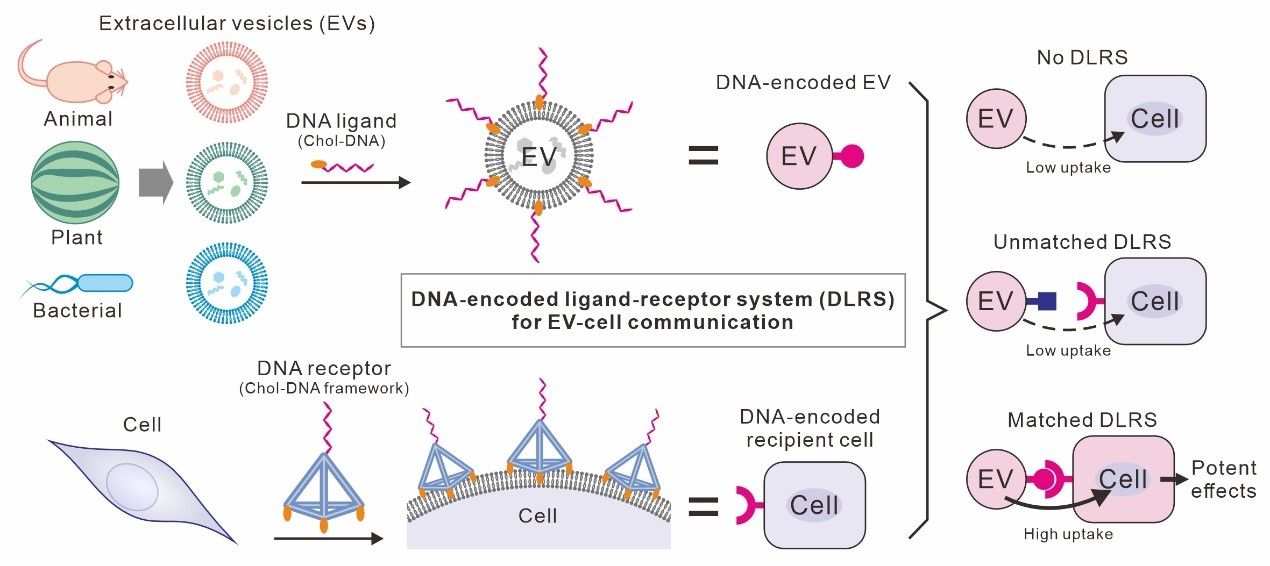
еӣҫ1. DNAзј–з Ғй…ҚдҪ“-еҸ—дҪ“зі»з»ҹд»ӢеҜјз»ҶиғһиЎЁеӣҠжіЎпјҲEVпјүдёҺз»Ҷиғһд№Ӣй—ҙзҡ„йҖҡи®Ҝ
й’ҲеҜ№иҝҷдёҖи®ҫжғі����пјҢй’»з ”еӣўйҳҹејҖеҸ‘дәҶдёҖз§ҚDNAзј–з Ғзҡ„дәәдёәй…ҚдҪ“-еҸ—дҪ“зі»з»ҹ����пјҢйҖҡиҝҮйқһе…ұд»·ж–№ејҸеҲ«зҰ»йғЁзҪІдәҺдҪңдёәдҫӣдҪ“зҡ„з»ҶиғһиЎЁеӣҠжіЎдёҺдҪңдёәеҸ—дҪ“зҡ„з»ҶиғһиЎЁиЎЁ�����гҖӮиҝҷж ·����пјҢз»ҶиғһиЎЁеӣҠжіЎдёҺеҸ—дҪ“з»ҶиғһиғҪеӨҹйҖҡиҝҮDNAзўұеҹәдә’иЎҘй…ҚеҜ№зү№ејӮжҖ§ең°з»“еҗҲ����пјҢд»ӢеҜјжӢҘжңүжӯЈдәӨжҖ§зҡ„з»ҶиғһиЎЁеӣҠжіЎ-з»Ҷиғһзӣёдә’дҪңз”ЁпјҲеӣҫ1пјү������������пјӣиҜҹеӯҹдҪҺ����пјҢй’»з ”еӣўйҳҹжҲҗеҠҹе®һзҺ°дәҶиө·жәҗдәҺеҲҶжӯ§зү©з§ҚпјҲе№јйј гҖҒиҘҝз“ңе’ҢеӨ§иӮ жқҶиҸҢпјүзҡ„з»ҶиғһиЎЁеӣҠжіЎдёҺдәәжәҗз»Ҷиғһд№Ӣй—ҙзҡ„и·Ёзү©з§ҚйҖҡи®Ҝ�����гҖӮиҜҘзі»з»ҹеңЁеӨҚжқӮз»ҶиғһзҺҜеўғдёӯжӢҘжңүеҫҲеҘҪзҡ„жӯЈдәӨжҖ§����пјҢеӣ иҖҢиғҪеӨҹжһ„е»әзІҫзЎ®зҡ„з»ҶиғһиЎЁеӣҠжіЎ-з»ҶиғһйҖҡи®Ҝеӣһи·Ҝ�����гҖӮжңҖз»Ҳ����пјҢиҜҘзі»з»ҹиў«жҲҗеҠҹеҲ©з”ЁдәҺжһ„е»әзҒөй•ҝзұ»еҠЁзү©йӣҢжҖ§з”ҹж®–е№Із»Ҷиғһзҡ„з»ҶиғһйҫӣпјҲеӣҫ2пјү����пјҢе®һзҺ°дәҶж— йңҖиұўе…»еұӮз»Ҷиғһзҡ„е№Із»ҶиғһиҮӘжҲ‘жӣҙж–°дёҺе№ІжҖ§з»ҙжҢҒ����пјҢдёәйӣҢжҖ§з”ҹж®–е№Із»Ҷиғһзҡ„дҪ“иЎЁе·ҘзЁӢеҢ–еҲ©з”ЁжҸҗдҫӣдәҶж–°зҡ„е·Ҙе…·�����гҖӮ
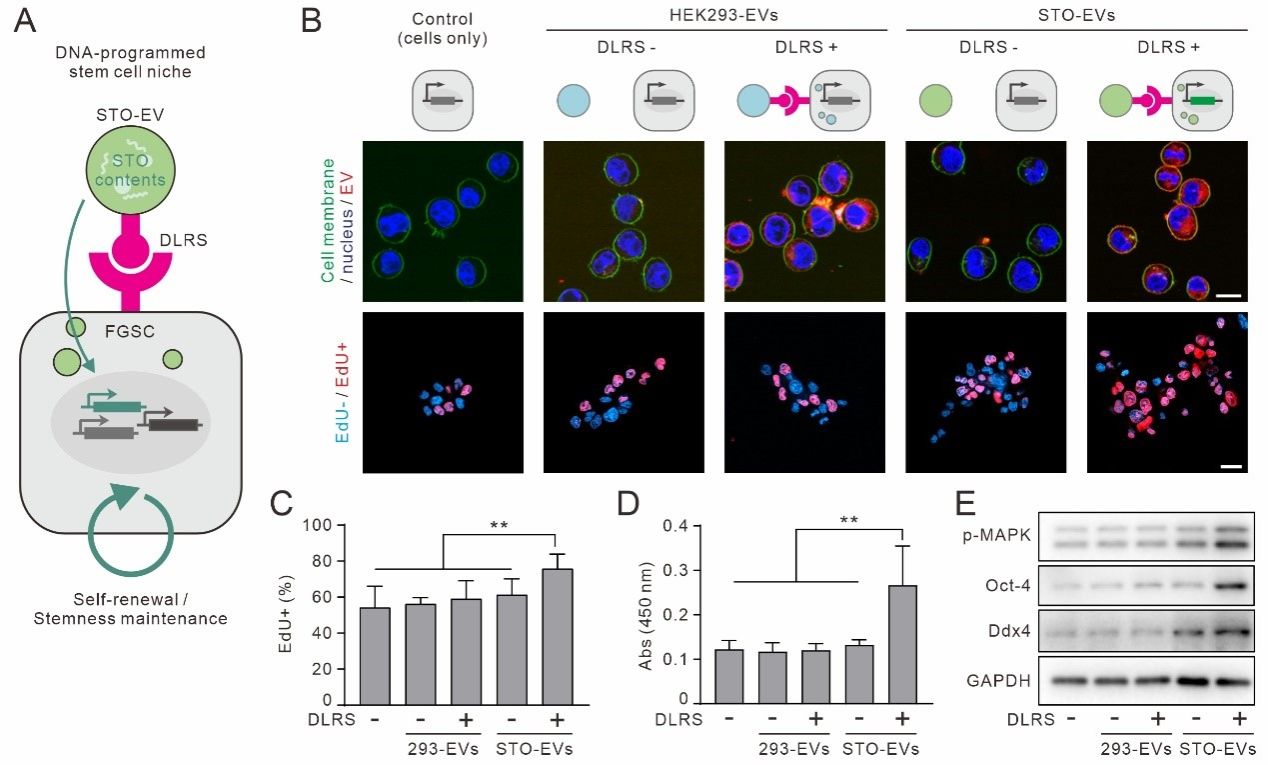
еӣҫ2. DNAзј–зЁӢз»ҶиғһиЎЁеӣҠжіЎдёҺе№Із»Ҷиғһзӣёдә’дҪңз”Ё����пјҢжһ„е»әйӣҢжҖ§з”ҹж®–е№Із»Ҷиғһйҫӣ
иҝҷйЎ№е·ҘдҪңдҫқйҷ„иҪ¬еҢ–еҢ»еӯҰеӣҪеәҰжІүеӨ§з§‘жҠҖеҹәзЎҖи®ҫж–Ҫ����пјҢдёҠиҝ°й’»з ”еҫ—еҲ°дәҶеӣҪеәҰжІүзӮ№з ”еҸ‘жү“з®—гҖҒеӣҪеәҰеӨ©з„¶з§‘еӯҰеҹәйҮ‘зӯүйЎ№дё»еј иөһеҠ©�����гҖӮ
и®әж–Үй“ҫжҺҘпјҡhttps://doi.org/10.1002/adma.202302323








