近日������,亿万先生MR性命科学学院、分子鉴别与生物传感钻研中心赵婧教授/曹亚高级尝试师团队在国际驰名期刊《Nature Communications》颁发题为“Homotypic membrane-powered electrochemical microfluidic analysis of extracellular vesicles for precise cancer diagnosis”的钻研成就�����。亿万先生MR性命科学学院硕士钻研生邹子涵和上海复旦大学从属肿瘤医院金希副钻研员为共同第一作者�����。亿万先生MR赵婧教授、曹亚高级尝试师和漯河师范大学王兆寅教授为论文的共同通讯作者�����。亿万先生MR为第一实现单元�����。
该钻研基于癌症细胞膜在分子层面保留亲本细胞特点的性质������,构建了一种新型生物仿生界面������,实现了乳腺癌细胞表囊泡(EVs)的亚型特异性精准分析�����。钻研了局批注������,该乳腺癌细胞膜仿生界面可能通过同型结合特异性鉴别并捕获拥有一样亚型特点的乳腺癌EVs������,进而实显熹高活络的电化学定量分析(图1)�����。该步骤对指标EVs亚型特点分析拥有高度的选择性和活络度������,能在乳腺癌患者血浆样本中正确区吩熹亚型特点������,展示出在乳腺癌精准诊断及液体活检方面的潜在利用价值�����。
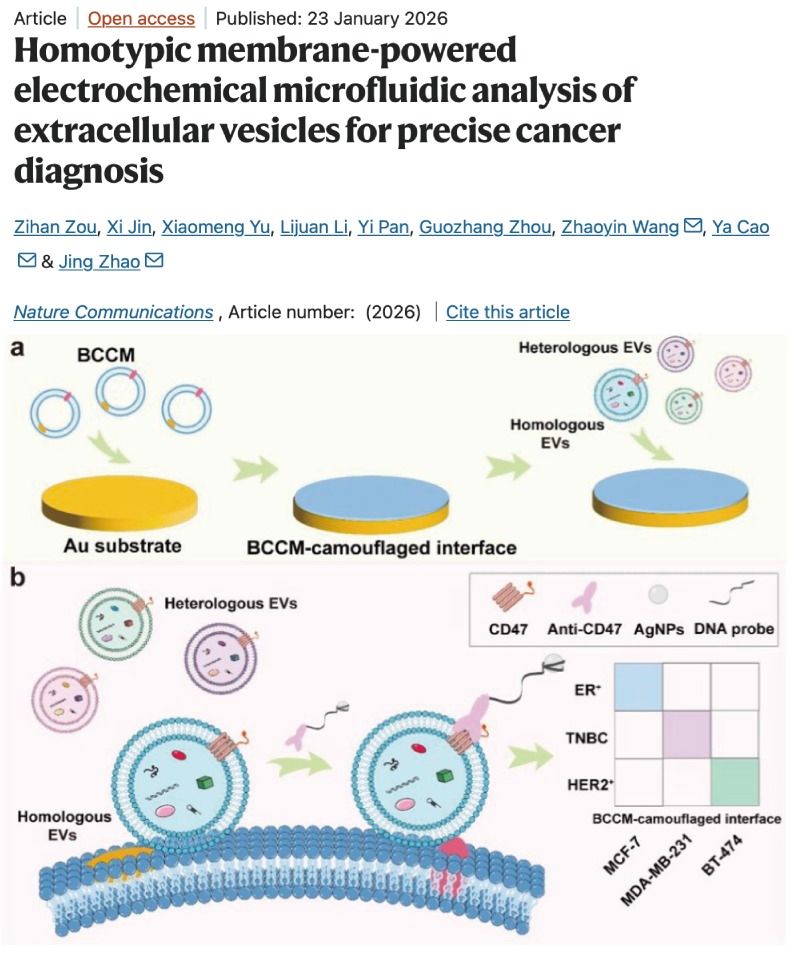
图1基于肿瘤细胞膜仿生界面同型鉴别性质的乳腺癌亚型诊断示意图
为实现高通量、自动化分析������,钻研团队进一步将该仿生界面与微流控技术相结合������,开发了一种四通路电化学微流控装置������,可同时平行分析多个样本�����。在90例乳腺癌患者、31例其他疾病患者及20例健全对照者的盲法测试中������,该微流控装置可能成功鉴别出与临床诊断一致的患者亚型特点������,为乳腺癌亚型特异性诊断提供了一种轻便、高效的平台������,也拓展了细胞膜假装战术在分子诊断领域的利用������,为实现更宽泛的癌症精准分型与个别化医治奠定了基�����。ㄍ2)�����。
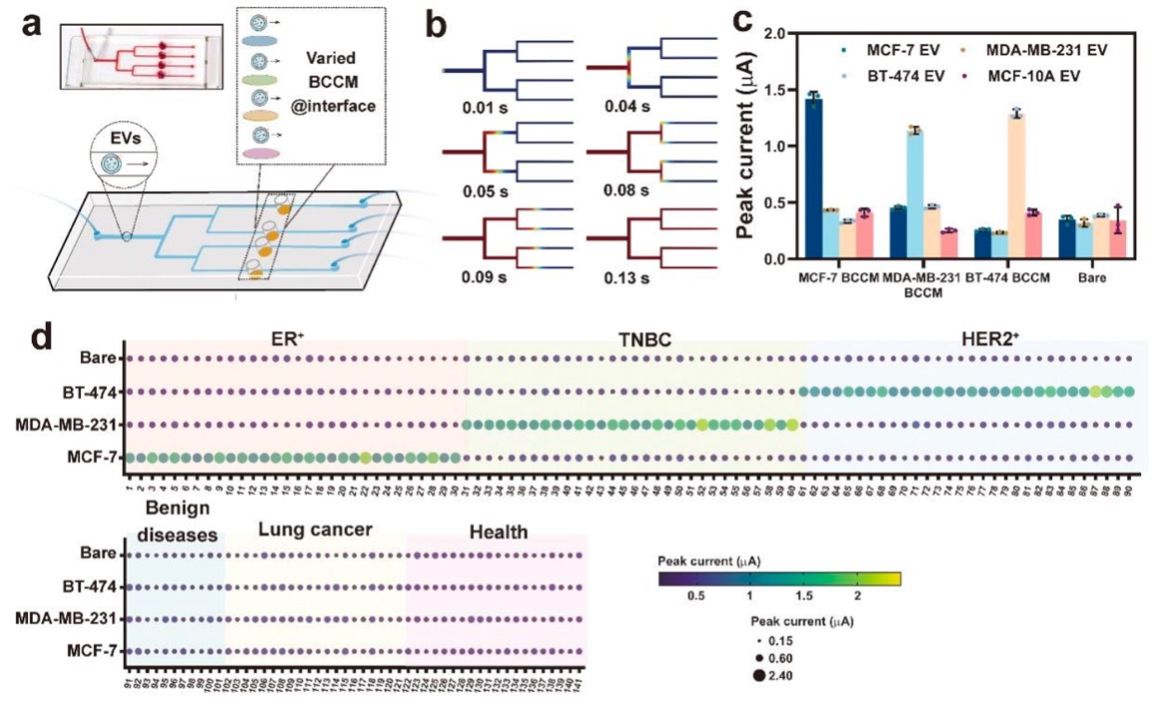
图2基于乳腺癌细胞膜仿生界面的肿瘤患者血浆样本微流控分析了局图�����。
同样聚焦乳腺癌精准分子分型钻研������,团队还与上海交通大学左幼磊钻研员、上海复旦大学从属肿瘤医院金希副钻研员合作������,在国际高水平期刊《Advanced Materials》颁发了题为“Cell surface-confined DNAzyme coordination-facilitated logical engineering for precise cell identification”的钻研成就(亿万先生MR为第一实现单元)�����。该钻研提出了一种基于细胞表表限域DNAzyme协同作用的细胞表型鉴别新战术������,可能利用G4 DNAzyme和RNA切割型DNAzyme(MNA)的协同作用������,实现逻辑门节造下特定表型细胞的高选择性象征与捕获�����。通过在乳腺癌干细胞亚群(如CD44?CD24?或同时表白EpCAM的亚群)中的验证钻研������,批注该技术可能通过多沉生物标志物的逻辑鉴别������,实现指标细胞的高效磁分离与电化学定量检测������,其正确性可与流式细胞术相媲美������,但是操作更为轻便������,并能结合Y形DNA探针等�����?������,实现多职能集成分析(图3)�����。

图3基于限域DNAzyme协同反映的乳腺癌细胞表型逻辑鉴别示意图
有关工作依附上海器官建复工程技术钻研中心������,得到国度天然科学基金(82470534、81972799、22222407、22176099)和上海市天然科学基金(23ZR1421400)等赞助�����。
论文下载链接:
https://www.nature.com/articles/s41467-026-68770-0
https://advanced.onlinelibrary.wiley.com/doi/10.1002/adma.202504363