近日��������,亿万先生MR医学院张天龙钻研员在性命科学权威期刊《Molecular Cell》(中科院一区��������,影响因子16.6)颁发题为“CASTOR1 and CASTOR2 respond to different arginine levels to regulate mTORC1 activity”的钻研成就��������,该钻研系统揭示了CASTOR1与CASTOR2作为高档真核生物特有的精氨酸感应蛋白��������,通过差距化响应细胞内分歧精氨酸浓度��������,调控GATOR2复合物职能及mTORC1活性��������,进而影响肌肉成长与分化��������,为肌肉萎缩、肿瘤等疾病的精准过问提供了新的理论凭据与潜在靶点������。

mTORC1信号通路是真核生物中高度守旧的营养感知主题��������,可能整合营养(尤其是氨基酸)与能量(ATP)供给状态��������,实时调控细胞合成代谢与分化代谢的动态平衡������。该通路异常与衰老、糖尿病、肥胖及肿瘤等多种沉大疾病的产生发展亲昵有关������。只管已知mTORC1活性受多种氨基酸调控��������,但细胞若何在氨基酸浓度颠簸下实现对mTORC1“动态、精密”响应��������,仍是领域内尚未解决的关键科学问题������。
在前期钻研中��������,团队解析了精氨酸感应蛋白CASTOR1-精氨酸复合物的晶体结构(CellDiscov., 2016)��������,发现CASTOR1对精氨酸拥有高亲和力(Kd≈ 5μM)��������,远低于正常生理前提下细胞中精氨酸浓度��������,提醒细胞必要依赖额表的感应机造以实现对精氨酸的梯度响应������。该钻研中��������,团队进一步聚焦CASTOR1的同源蛋白CASTOR2������。CASTOR2早期被以为不具备精氨酸结合能力��������,仅作为mTORC1的组成型负调控因子阐扬职能������。该钻研通过生化职能分析和复合物结构测定发现��������,CASTOR2同样可结合精氨酸��������,其亲和力显著低于CASTOR1(Kd≈ 215μM)��������,提醒其在高浓度精氨酸前提下阐扬调控作用������������;焐��������,CASTOR1与CASTOR2均可与GATOR2主题组分Mios直接结合��������,阻断GATOR2与GATOR1的相互作用��������,从而抑造mTORC1活性������。分歧浓度的精氨酸通过调控CASTOR1/2与Mios的结合强度��������,实现对GATOR1活性的梯度调控��������,进而精密调节mTORC1活性������。钻研进一步发现CASTOR1/2在肌肉组织中高表白��������,其介导的精氨酸感知机造直接影响肌肉细胞中mTORC1活性及细胞成长与分化过程������。
综上��������,该钻研初次提出CASTOR1/2作为“双沉传感器”协同作用��������,别离响应低浓杜纂高浓度精氨酸��������,实现对mTORC1活性的分段、梯度调控��������,突破了传统精氨酸营养信号响应的“开/关式”认知框架��������,也为理解细胞若何在颠簸的营养环境中维持代谢稳态提供了新的理论模式��������,为营养感知、代谢调控及有关疾病过问钻研启发了新的方向������。
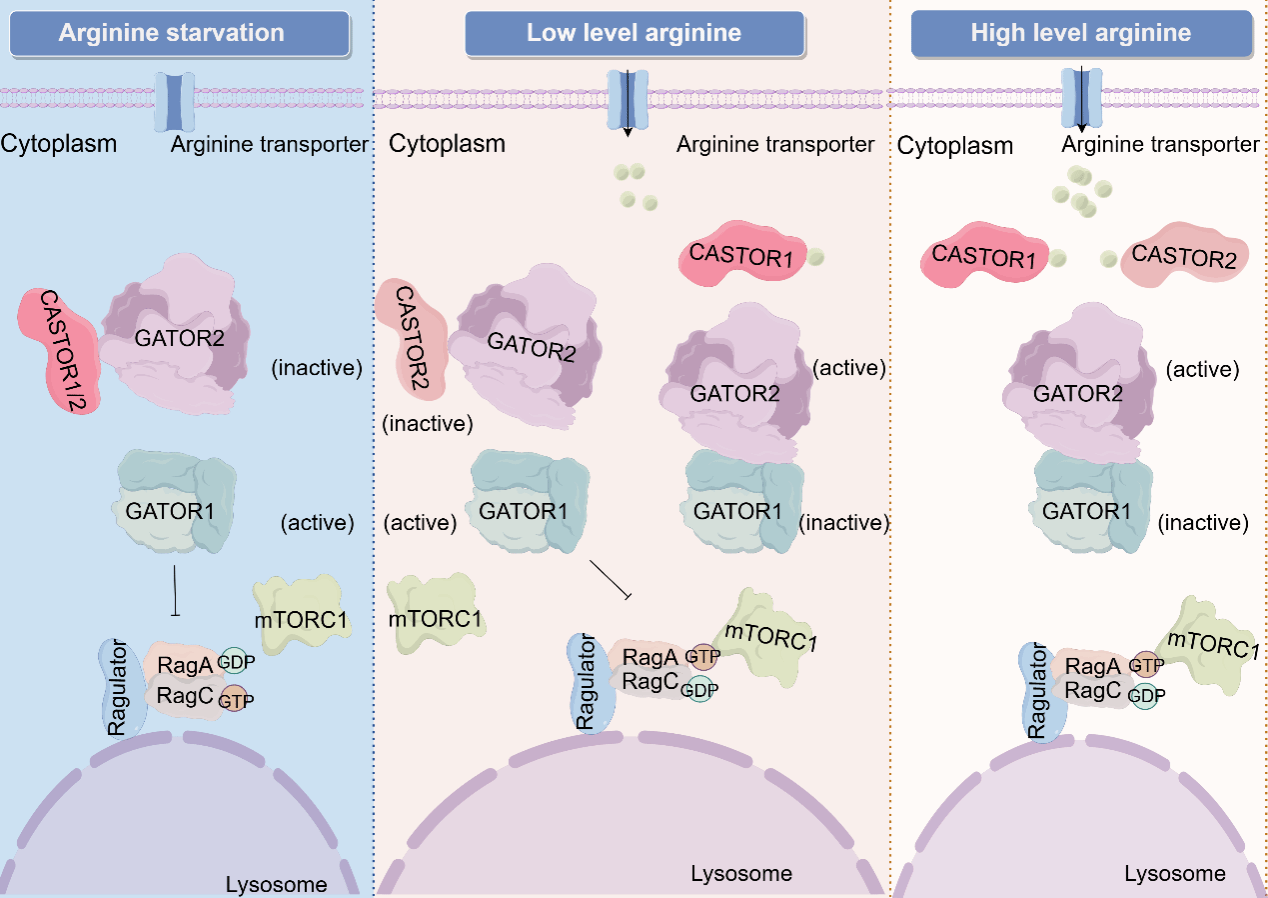
图1. CASTOR1/2的作用机造示意图������。当精氨酸不足时��������,CASTOR1和CASTOR2别离结合GATOR2复合物��������,抑造GATOR2与GATOR1的相互作用��������,GATOR1阐扬GAP活性��������,抑造下游Rag幼G蛋白与mTORC1的相互作用��������,从而抑造mTORC1活性������;当营养充足时��������,CASTOR1和CASTOR2别离响应低浓度和高浓度的精氨酸��������,从GATOR2解离��������,进而GATOR2抑造GATOR1活性��������,推进mTORC1与Rag幼G蛋白结合定位在溶酶体上��������,激活mTORC1信号通路������。
亿万先生MR医学院博士钻研生刘婵为该钻研的第一作者������。亿万先生MR医学院张天龙钻研员和中国科学院分子细胞科学卓越创新中心丁建平钻研员为论文的共同通讯作者������。该钻研得到了校内肖好汉、苏笠教授等团队和北京大学刘颖教授的领导支持������。该钻研获得科技部沉点研发打算、国度天然科学基金、亿万先生MR医学院科技创新基金和跨学科新医科钻研生创新基金等项主张赞助������。
原文链接:https://www.cell.com/molecular-cell/fulltext/S1097-2765(25)01015-9